當(dāng)我們進(jìn)行高強度的“擼鐵”訓(xùn)練后,往往會出現(xiàn)肌肉酸痛,而休息兩天后又變得生龍活虎,這是因為肌肉干細(xì)胞可以與受損肌細(xì)胞融合或者生產(chǎn)新的肌纖維。近期,來自西班牙龐培法布拉大學(xué)的William Roman等人發(fā)現(xiàn)了一種肌細(xì)胞自我修復(fù)的全新機制,它不依靠肌肉干細(xì)胞,而是肌纖維通過細(xì)胞核的遷移,實現(xiàn)損傷后的再生。相關(guān)研究于2021年10月15日發(fā)表在Science期刊上,題為“Muscle repair after physiological damage relies on nuclear migrationfor cellular reconstruction”。
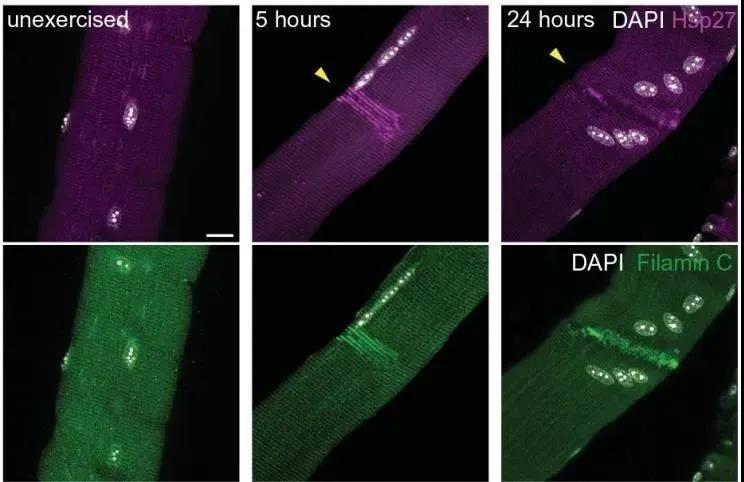
與人體內(nèi)大多數(shù)細(xì)胞不同的是,肌肉細(xì)胞由多個成肌細(xì)胞融合而來,因此一個肌細(xì)胞擁有多個細(xì)胞核。肌肉的過度收縮會造成肌纖維的損傷,但是很快肌纖維可以完成自我修復(fù)。為了研究這一過程,研究人員構(gòu)建了小鼠的運動模型,經(jīng)過5小時的運動,在小鼠腿部比目魚肌的受損區(qū)域發(fā)現(xiàn)了細(xì)絲蛋白C(FLNC)和熱休克蛋白27(HSP27)的聚集,這有助于受損部位的愈合;而在運動48小時后,這些蛋白的聚集幾乎消失,這說明在此之前已經(jīng)迅速完成了肌肉修復(fù)。而且在這個過程中,沒有檢測到肌肉干細(xì)胞的參與。
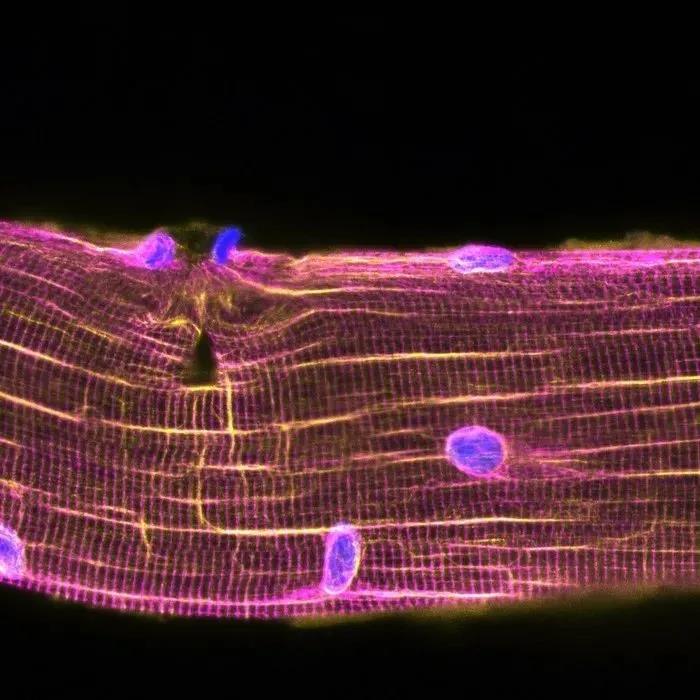
此外,在體外培養(yǎng)的肌細(xì)胞模型中,研究人員發(fā)現(xiàn),在受損后肌纖維的細(xì)胞核陸續(xù)向受損區(qū)域遷移。5小時內(nèi),73%的細(xì)胞核都聚集在受損區(qū)域附近。這直接導(dǎo)致了mRNA分子的局部遞送,這些mRNA在受損區(qū)域被翻譯形成FLNC、HSP27等,是肌肉修復(fù)良好的原材料。同時,研究人員發(fā)現(xiàn)了一條與鈣離子相關(guān)的、負(fù)責(zé)調(diào)控細(xì)胞的運動的信號通路:細(xì)胞分裂周期蛋白42(CDC42)。當(dāng)抑制CDC42時,細(xì)胞核的遷移隨之受到抑制;反之,激活CDC42,未受損肌纖維中的細(xì)胞核仍會移動。因此,肌肉細(xì)胞的這種自我修復(fù)機制是通過CDC42的調(diào)控實現(xiàn)的。
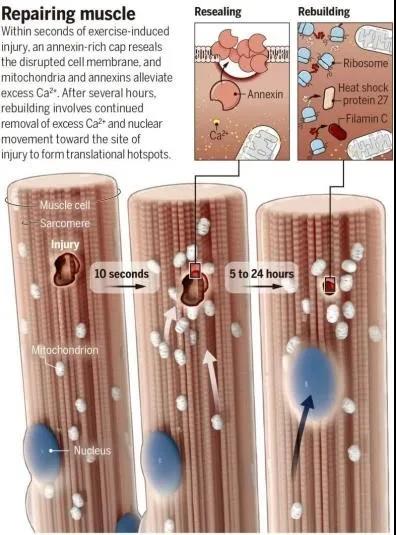
總之,研究發(fā)現(xiàn),運動所致的局部肌肉損傷會激活一種不依賴于肌肉干細(xì)胞的肌纖維自我修復(fù)機制。小鼠的肌肉損傷觸發(fā)了涉及鈣離子、CDC42和磷酸激酶C的信號級聯(lián)反應(yīng),并通過微管和動力蛋白將細(xì)胞核吸引到受損部位。細(xì)胞核的遷移加速了肌纖維的修復(fù),在局部遞送mRNA以進(jìn)行肌細(xì)胞的重建。這種細(xì)胞自主的保護(hù)機制是我們更全面、更深入地了解生理和疾病中的肌肉修復(fù)的一種替代模型。而《科學(xué)》雜志同期的一篇展望文章則認(rèn)為,這個發(fā)現(xiàn)還有著更為深遠(yuǎn)的意義:在這項研究中出現(xiàn)的關(guān)鍵蛋白,例如HSP27、CDC42,有可能成為修復(fù)損傷或幫助患者康復(fù)的新靶點。
 |
 |
 |
| 官網(wǎng):www.baichuan365.com |
微信服務(wù)號:iseebio |
微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn |
微信訂閱號:seebiotech |
泉養(yǎng)堂:www.canmedo.com |